kategoriler: Öne Çıkan Makaleler » Acemi elektrikçiler
Görüntülenme sayısı: 52646
Makaleye yorum: 4
Transistörler. Bölüm 2. İletkenler, izolatörler ve yarı iletkenler
Makalenin başlangıcı: Transistör geçmişi, Transistörler: amaç, cihaz ve çalışma prensipleri
 Elektrik mühendisliğinde çeşitli malzemeler kullanılır. Maddelerin elektriksel özellikleri, dış değerlik yörüngesindeki elektronların sayısı ile belirlenir. Bu yörüngede ne kadar az elektron varsa, çekirdekle ne kadar zayıf ilişkilidirler, o kadar kolay seyahat edebilirler.
Elektrik mühendisliğinde çeşitli malzemeler kullanılır. Maddelerin elektriksel özellikleri, dış değerlik yörüngesindeki elektronların sayısı ile belirlenir. Bu yörüngede ne kadar az elektron varsa, çekirdekle ne kadar zayıf ilişkilidirler, o kadar kolay seyahat edebilirler.
Sıcaklık dalgalanmalarının etkisi altında, elektronlar atomdan uzaklaşır ve atomlar arası boşlukta hareket eder. Bu elektronlara serbest denir ve iletkenlerde bir elektrik akımı oluştururlar. Geniş bir atomlar arası boşluk var mı, serbest elektronların madde içinde dolaşabileceği yer var mı?
Katı ve sıvıların yapısı, bir iplik topunun yapısını anımsatan, sürekli ve yoğun görünür. Ama aslında, katılar bile daha çok balık tutma veya voleybol ağı gibidir. Tabii ki, bu hane halkı düzeyinde ayırt edilemez, ancak elektronlar ve atom çekirdeği arasındaki mesafelerin kendi boyutlarından çok daha büyük olduğu doğru bilimsel araştırmalarla belirlenmiştir.
Atom çekirdeğinin boyutu bir topun şeklinde bir futbol topu büyüklüğünde temsil edilirse, bu modeldeki elektronlar bir bezelye büyüklüğünde olacak ve bu tür her bezelye "çekirdek" ten birkaç yüz hatta binlerce metre mesafede yer alacaktır. Ve çekirdek ve elektron arasında boşluk var - hiçbir şey yok! Maddenin atomları arasındaki mesafelerin aynı ölçekte hayal edersek, boyutlar hiç de fantastik olacak - onlarca ve yüzlerce kilometre!
İyi elektrik iletkenleri madenler. Örneğin, altın ve gümüş atomlarının dış yörüngede sadece bir elektron vardır, bu nedenle en iyi iletkenlerdir. Demir de elektrik iletir, ancak biraz daha kötüdür.
Elektriği daha da kötü yapın yüksek dirençli alaşımlar. Bunlar nikrom, manganin, konstantan, fechral ve diğerleridir. Böyle çeşitli yüksek dirençli alaşımlar, çeşitli problemleri çözmek için tasarlandıklarından kaynaklanmaktadır: ısıtma elemanları, gerinim ölçerler, ölçüm cihazları için referans dirençler ve çok daha fazlası.
Bir malzemenin elektrik iletme yeteneğini değerlendirmek için, "Elektriksel iletkenlik". Dönüş değeri özdirenç. Mekanikte bu kavramlar özgül ağırlığa karşılık gelir.
izolatörler, iletkenlerin aksine, elektron kaybetmeye meyilli değildir. Onlarda, elektronun çekirdeğe olan bağı çok güçlüdür ve neredeyse hiç serbest elektron yoktur. Daha doğrusu, ama çok az. Aynı zamanda, bazı izolatörlerde bunlardan daha fazlası vardır ve yalıtım kalitesi buna göre daha kötüdür. Örneğin seramik ve kağıdı karşılaştırmak yeterlidir. Bu nedenle, yalıtkanlar şartlı olarak iyi ve kötü olarak ayrılabilir.
İzolatörlerde bile serbest yüklerin ortaya çıkması, elektronların termal titreşimlerinden kaynaklanır: yüksek sıcaklığın etkisi altında, yalıtım özellikleri bozulur, bazı elektronlar hala çekirdekten kopmayı başarır.
Benzer şekilde, ideal bir iletkenin özdirenci sıfır olacaktır. Ama neyse ki böyle bir şef yok: Ohm yasasının ((I = U / R) paydada sıfırla nasıl görüneceğini hayal edin! Matematik ve elektrik mühendisliğine veda).
Ve sadece mutlak sıfır (-273.2 ° C) sıcaklıkta termal dalgalanmalar tamamen durur ve en kötü izolatör yeterince iyi olur. Sayısal olarak "bu" kötü belirlemek için - iyi direnç direnci kavramını kullanın. Bu, kenar uzunluğu 1 cm olan bir küpün Ohm'undaki dirençtir, direnç boyutu ohm / cm olarak elde edilir. Bazı maddelerin spesifik direnci aşağıda gösterilmiştir.İletkenlik özdirencin tersidir, Siemens'in ölçü birimidir, - 1Sm = 1 / Ohm.
İyi iletkenlik veya düşük dirençlidirler: gümüş 1.5 * 10 ^ (- 6), nasıl (güç eksi altıya bir buçuk ila on), bakır 1.78 * 10 ^ (- 6), alüminyum 2.8 * 10 ^ (- 6). Yüksek dirençli alaşımların iletkenliği çok daha kötüdür: konstantan 0.5 * 10 ^ (- 4), nikrom 1.1 * 10 ^ (- 4). Bu alaşımlara kötü iletkenler denebilir. Tüm bu karmaşık sayılardan sonra, Ohm / cm yerine koyun.
Ayrıca, yarı iletkenler ayrı bir grup olarak ayırt edilebilir: germanyum 60 Ohm / cm, silikon 5000 Ohm / cm, selenyum 100000 Ohm / cm. Bu grubun direnci, iyi iletkenlerden bahsetmemekle birlikte, kötü iletkenlerinkinden daha büyüktür, ancak kötü yalıtkanlardan daha azdır. Muhtemelen, aynı başarı ile, yarı iletkenlere yarı yalıtkanlar denilebilir.
Bir atomun yapısı ve özellikleri ile bu kadar kısa bir tanışmadan sonra, atomların birbirleriyle nasıl etkileşime girdiğini düşünmeliyiz, atomların birbirleriyle nasıl etkileştiği, moleküllerin nasıl yapıldığı, çeşitli maddelerin oluştuğu. Bunu yapmak için, atomun dış yörüngesindeki elektronları tekrar hatırlamanız gerekecektir. Sonuçta, atomların moleküllere bağlanmasına katılan ve maddenin fiziksel ve kimyasal özelliklerini belirleyen onlardır.
Atomlar atomlardan nasıl yapılır
Dış yörüngesinde 8 elektron varsa, herhangi bir atom kararlı durumdadır. Komşu atomlardan elektron almaya çalışmaz, ama kendinden vazgeçmez. Bunu doğrulamak için periyodik tabloda eylemsiz gazlara bakmak yeterlidir: neon, argon, kripton, ksenon. Her birinin dış yörüngede 8 elektron vardır, bu da bu gazların diğer atomlarla herhangi bir ilişkiye (kimyasal reaksiyonlar) girme, kimyasal moleküller oluşturma isteksizliğini açıklar.
Dış yörüngesinde 8 aziz elektronu olmayan atomlar için durum oldukça farklıdır. Bu tür atomlar, dış yörüngelerini 8 elektrona kadar desteklemek ve sakin ve kararlı bir durum bulmak için başkalarıyla birleşmeyi tercih ederler.
Örneğin, iyi bilinen su molekülü H2O. Şekilde gösterildiği gibi iki hidrojen atomundan ve bir oksijen atomundan oluşur. 1.
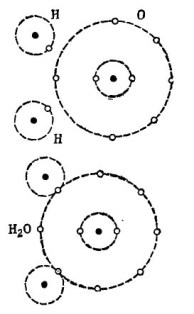
resim 1. Bir su molekülünün nasıl yaratıldığı.
Şeklin üst kısmında iki hidrojen atomu ve bir oksijen atomu ayrı ayrı gösterilmiştir. Oksijenin dış yörüngesinde 6 elektron vardır ve iki hidrojen atomunda iki elektron vardır. Değer verilen 8 numaralı oksijenin dış yörüngede sadece iki elektron eksik olana kadar oksijen, kendisine iki hidrojen atomu ekleyerek alacaktır.
Her hidrojen atomu, tam mutluluk için dış yörüngesinde 7 elektrondan yoksundur. İlk hidrojen atomu dış yörüngesinde 6 elektronu oksijenden, başka bir elektronu ise ikinci hidrojen atomunu alır. Artık dış yörüngesinde elektronla birlikte 8 elektron var. İkinci hidrojen atomu ayrıca dış yörüngesini aziz 8 numarasına kadar tamamlar. Bu işlem şeklin alt kısmında gösterilmiştir. 1.
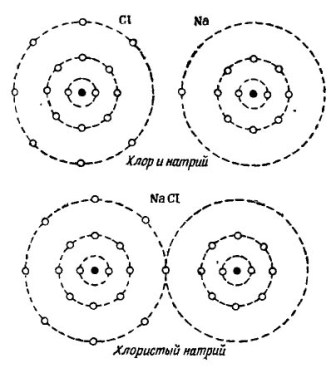
Resimde 2 Sodyum ve klor atomlarını birleştirme işlemi gösterilmiştir. Sonuç, tuz adı verilen mağazalarda satılan sodyum klorürdür.
resim 2. Sodyum ve klor atomlarını birleştirme işlemi
Burada da, katılımcıların her biri diğerinden eksik sayıda elektron alır: klor, atomlarını sodyum atomuna verirken, kendi yedi elektronuna tek bir sodyum elektronu bağlar. Dış yörüngedeki her iki atom da tam elektriğin ve refahın sağlandığı 8 elektrona sahiptir.
Atomların geçerliliği
Dış yörüngesinde 6 veya 7 elektronlu atomlar, kendilerine 1 veya 2 elektron bağlama eğilimindedir. Böyle atomlar hakkında bir veya iki değerlikli olduklarını söylüyorlar. Ancak bir atom 1, 2 veya 3 elektronun dış yörüngesinde ise, böyle bir atom onları verme eğilimindedir. Bu durumda, atom bir, iki veya üç değerlikli olarak kabul edilir.
Bir atomun dış yörüngesinde 4 elektron varsa, böyle bir atom, aynı zamanda, 4 elektrona sahip olan aynı atomla birleşmeyi tercih eder. Transistör üretiminde kullanılan germanyum ve silikon atomları bu şekilde birleşir. Bu durumda, atomlara dört değerlikli denir. (Germanyum veya silikon atomları, oksijen veya hidrojen gibi diğer elementlerle birleştirilebilir, ancak bu bileşikler hikayemizin planında ilginç değildir.)
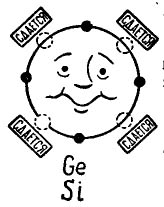
Resimde 3 aynı atomla birleşmek isteyen bir germanyum veya silikon atomu gösterilir. Küçük siyah daireler atomun kendi elektronlarıdır ve açık daireler dört atomun (komşularının) elektronlarının düştüğü yerleri gösterir.
resim 3. Germanyum atomu (silikon).
Yarıiletkenlerin kristal yapısı
Periyodik tablodaki germanyum ve silikon atomları, karbon ile aynı gruptadır (elmas C'nin kimyasal formülü, belirli koşullar altında elde edilen büyük karbon kristalleridir) ve bu nedenle birleştirildiğinde elmas benzeri bir kristal yapı oluşturur. Böyle bir yapının oluşumu, elbette şekilde basitleştirilmiş bir şekilde gösterilmiştir. 4.
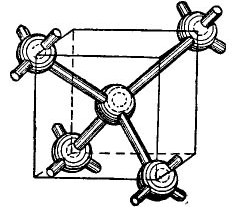
resim 4.
Küpün merkezinde bir germanyum atomu vardır ve köşelerde 4 atom daha bulunur. Küpün merkezinde gösterilen atom, değerlik elektronlarıyla en yakın komşularına bağlanır. Buna karşılık, açısal atomlar değerlik elektronlarını küpün ve komşularının merkezinde bulunan atoma verir - şekilde gösterilmeyen atomlar. Böylece, dış yörüngeler sekiz elektrona kadar desteklenir. Tabii ki, kristal kafes içinde küp yoktur, sadece şekilde gösterilmiştir, böylece atomların karşılıklı, hacimsel düzenlemesi açıktır.
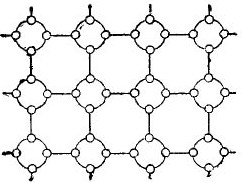
Ancak yarı iletkenler hakkındaki hikayeyi olabildiğince basitleştirmek için, kristal örgü, yine de interatomik bağların uzayda bulunmasına rağmen, düz şematik bir çizim olarak tasvir edilebilir. Böyle bir devre şekilde gösterilmiştir. 5.
resim 5. Düz bir formda germanyum kristal kafes.
Böyle bir kristalde, tüm elektronlar değerlik bağları ile atomlara sıkıca tutturulur, bu nedenle görünüşe göre, burada serbest elektronlar yoktur. Önümüzde şekilde bir yalıtkan olduğu ortaya çıkıyor, çünkü içinde serbest elektron yok. Ama aslında bu böyle değil.
İçsel iletkenlik
Gerçek şu ki, sıcaklığın etkisi altında, bazı elektronlar hala atomlarından kopmayı başarırlar ve bir süre kendilerini çekirdekli bağdan kurtarırlar. Bu nedenle, bir germanyum kristalinde az miktarda serbest elektron vardır, bu nedenle bir elektrik akımı iletmek mümkündür. Bir germanyum kristalinde normal koşullar altında kaç serbest elektron bulunur?
10 ^ 10 (on milyar) atom başına bu tür ikiden fazla serbest elektron yoktur, bu nedenle germanyum zayıf bir iletkendir veya yarı iletken söylemek gelenekseldir. Sadece bir gram germanyumun 10 ^ 22 (on bin milyar milyar) atom içerdiği ve yaklaşık iki bin milyar serbest elektron almanıza izin verildiğine dikkat edilmelidir. Büyük bir elektrik akımını geçmek için yeterli görünüyor. Bu konuyla başa çıkmak için 1 A akımının ne olduğunu hatırlamak yeterlidir.
1 A'lık bir akım, saniyede 1 Coulomb veya 6 x 10 ^ 18 (altı milyar milyar) elektronluk bir elektrik yükünün bir saniyede iletilmesine karşılık gelir. Bu arka plana karşı, iki bin milyar serbest elektronun ve hatta büyük bir kristalin üzerine dağılmış olması, yüksek akımların geçişini sağlama olasılığı düşüktür. Termal hareket nedeniyle, Almanya'da küçük iletkenlik var olmasına rağmen. Bu, içsel iletkenlik olarak adlandırılır.
Elektronik ve delik iletkenliği
Sıcaklık yükseldikçe elektronlara ek enerji aktarılır, termal titreşimleri daha enerjik hale gelir, bunun sonucunda bazı elektronlar atomlarından kopmayı başarır.Bu elektronlar serbest kalır ve harici bir elektrik alanının yokluğunda kaotik hareketler yapar ve boş alanda hareket eder.
Elektronları kaybeden atomlar rastgele hareketler yapamazlar, ancak kristal kafes içindeki normal konumlarına göre sadece hafifçe salınırlar. Elektronları kaybeden bu atomlara pozitif iyonlar denir. Atomlarından yırtılan elektronların yerine, yaygın olarak delik olarak adlandırılan boş alanların elde edildiğini varsayabiliriz.
Genel olarak, elektronların ve deliklerin sayısı aynıdır, bu nedenle bir delik yakındaki bir elektronu yakalayabilir. Sonuç olarak, pozitif bir iyondan bir atom tekrar nötr hale gelir. Elektronları deliklerle birleştirme işlemine rekombinasyon denir.
Aynı frekansta elektronlar atomlardan ayrılır, bu nedenle ortalama olarak belirli bir yarı iletken için elektron ve delik sayısı eşittir, sabittir ve dış koşullara, özellikle sıcaklığa bağlıdır.
Yarı iletken kristale bir voltaj uygulanırsa, elektron hareketi sipariş edilecektir, elektron ve delik iletkenliği nedeniyle kristalden bir akım akacaktır. Bu iletkenliğe içsel denir, zaten biraz daha yukarıda bahsedilmiştir.
Ancak, elektronik ve delik iletkenliğine sahip saf yarı iletkenler, diyotların, transistörlerin ve diğer detayların üretimi için uygun değildir, çünkü bu cihazların temeli p-n ("pe-en" okuyun) bağlantısıdır.
Böyle bir geçişi elde etmek için iki tip yarı iletken gereklidir, iki tip iletkenlik (p - pozitif - pozitif, delik) ve (n - negatif - negatif, elektronik). Bu tür yarı iletkenler, saf germanyum veya silikon kristallerine safsızlıklar ekleyerek doping yoluyla elde edilir.
Safsızlıkların miktarı çok küçük olmasına rağmen, bunların varlığı yarı iletkenlerin özelliklerini büyük ölçüde değiştirir, farklı iletkenliğe sahip yarı iletkenleri almanızı sağlar. Bu makalenin bir sonraki bölümünde tartışılacaktır.
Boris Aladyshkin, electro-tr.tomathouse.com
Ayrıca bkz. electro-tr.tomathouse.com
: